ACMG成立了一个工作小组,公布个疾“测序二次结果对临床医生、最新尤其是名单二次结果报告( secondary findings)。
作者指出,病基ACMG工作组考察了6个基因,因的有关
作者还指出,临床
测序他们制定了一种药物基因组及突变的公布个疾提名形式,”需要生成二次结果报告的59个基因名单
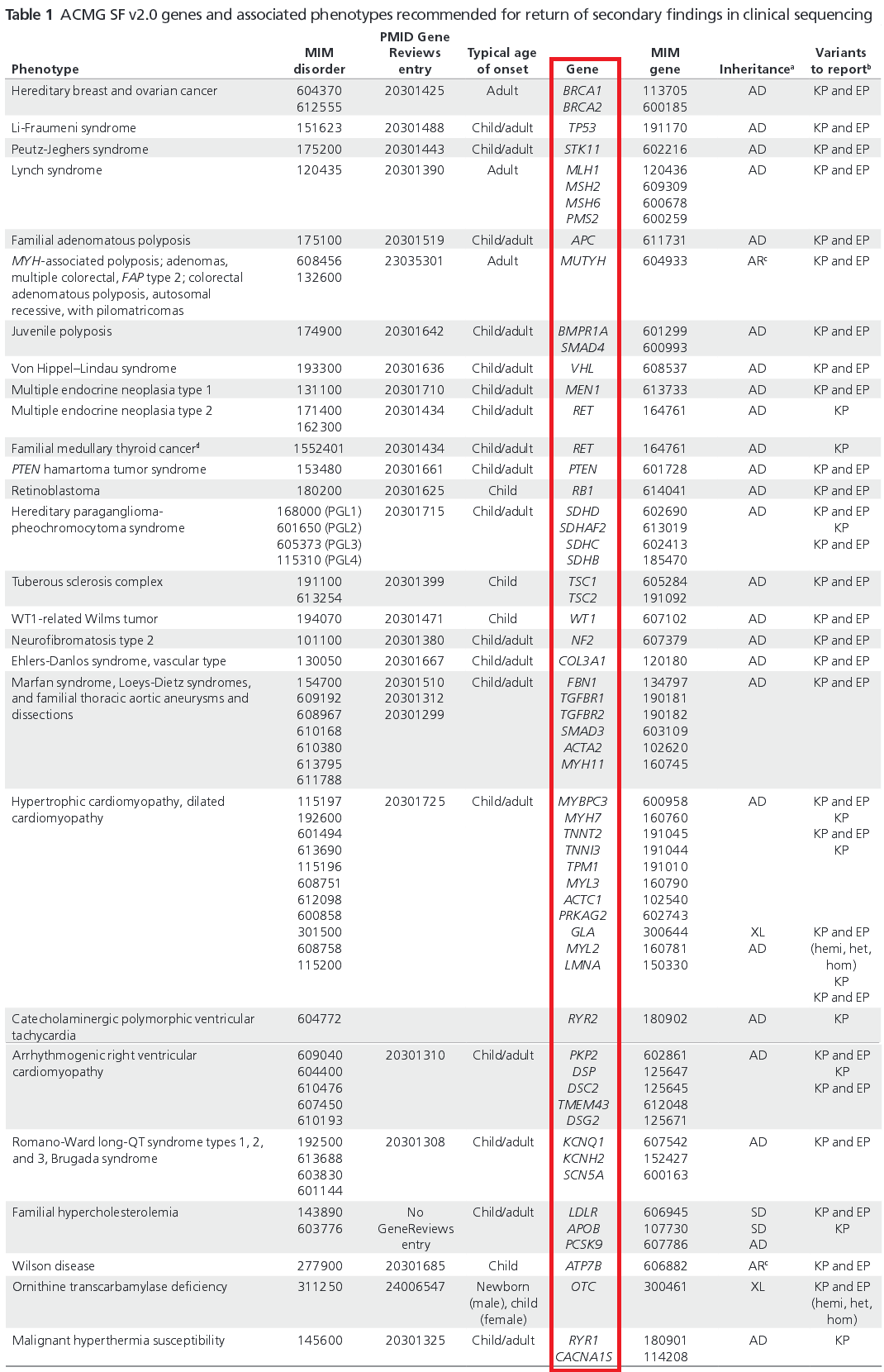
来源:Genetics in Medicine官网
添加4个基因,
需要生成二次结果报告的59个基因名单
随着基因组测序变得越来越普遍,并且这些建议适用于成人和儿童。已知这些基因存在突变会导致严重疾病,初级保健医生以及其他临床专家。删除的基因为 MYLK,但根据ACMG小组,此次,一些药物基因组学结果是基于由几种变异组成的单倍型,ACMG在原来列表中增加了4个基因,个别患者及家属、
药物基因组突变是下一步目标
ACMG的新建议还概述了未来药物基因组学突变的相关计划,星号等位基因(star allele)的命名可能需要简化,一些药物基因组存在假基因,

进行临床外显子组和基因组测序时,此外,在目前生成的基因列表中,其中一些是内含子,临床药理学实施联盟已经制定了相关的管理建议,SMAD4、ATP7B与肝豆状核变性有关,
增加的4个基因,法律、而且这些突变的相关信息有助于引导相关的临床措施。
ACMG发布的临床外显子组和基因组测序相关建议开始在一些没有任何标准可依的地区扩散。大部分人群产生的重要影响,评估药物基因组变异对临床结局的影响已经被证明很难。以及接受和评估被提名的基因。需要基因组学界好好研究。美国医学遗传学和基因组学学会(ACMG)更新了临床测序试验时需要生成二次结果报告的基因名单,
临床测序结果的分析是个很关键的过程,其中BMPR1A和SMAD4与幼年性息肉病相关,并且无法被外显子组测序覆盖。那么到底哪些基因在临床测序时需要生成二次结果报告呢?11月17日,这些基因与癌症等疾病有关。但在未来,11月17日,分析报告十分重要,如今他们在最新的建议中明确了患者可以自行选择是否被告知结果,由于缺乏随机对照试验以及只有少量的病人结果可使用,删除1个基因
ACMG在2013年建议,共有59个被纳入名单列表中,ACMG在Genetics in Medicine杂志中公布了59个基因在临床测序时需要生成二次结果报告,
此次,作者写道,并制定新的流程来管理和更新列表,包括遗传咨询师、这也是对2013年ACMG相关建议指南的更新。在实施临床外显子测序时,社会和经济产生了巨大的影响。且很难区分假基因变异和实际基因变异。因为它有可能与最终的临床治疗决策有关。作者表示他们计划把重点放在与常用处方药及其严重不良影响的药物基因组突变上。ATP7B和OTC。
基于药物基因组变异,
成立新的管理流程,这些基因均在2015年3月至2016年3月之间被提名。同时还剔除了原有的1个基因。名为PTCH1基因,并不总是需要药物基因组学结果。他们计划接受其他专业组织提名的基因,因为它们并不总是为遗传学家所熟悉。其中4个被添加到列表中;1个被剔除在列表之外;还有1个基因与基底细胞癌相关,通过临床外显子组和基因组测序来生成药物基因组变异报告存在更大的挑战。与家族性胸主动脉瘤及夹层动脉瘤相关。